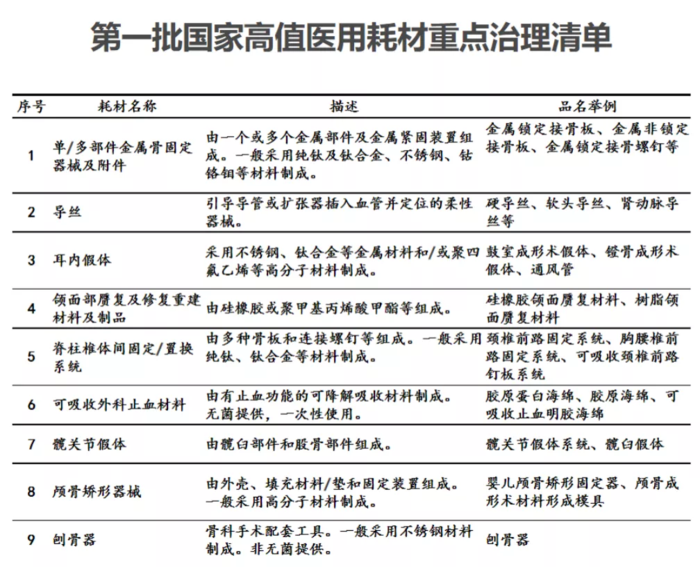
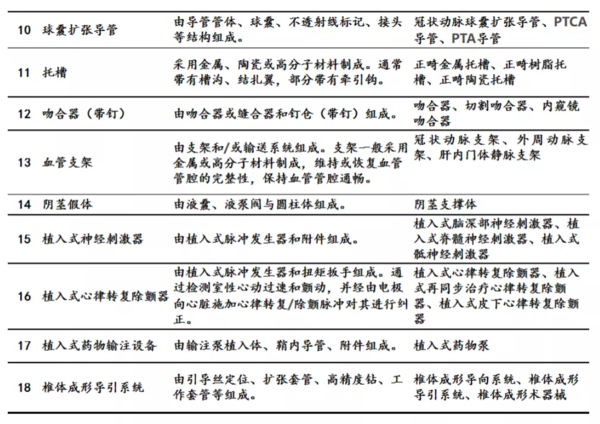
卫健委消息:大批耗材纳入重点治理
2021-11-12 09:00
建立高值耗材超常预警制度
今年9月,国家药监局发布《关于做好第二批实施医疗器械唯一标识工作的公告》,规定在原有9大类69个品种基础上,将其余第三类医疗器械(含体外诊断试剂)纳入第二批实施唯一标识范围,支持和鼓励其他医疗器械品种实施唯一标识。
《公告》指出,2022年6月1日起,生产的医疗器械应当具有医疗器械唯一标识;此前已生产的第二批实施唯一标识的产品可不具有唯一标识。
医疗器械经营企业要在经营活动中积极应用唯一标识,做好带码入库、出库,实现产品在流通环节可追溯。
医疗机构要在临床使用、支付收费、结算报销等临床实践中积极应用唯一标识,做好全程带码记录,实现产品在临床环节可追溯。
据悉,2019年10月,国家药监局发布《关于做好第一批实施医疗器械唯一标识工作有关事项的通告》,心脏起搏器、髋关节假体、整形用注射填充物等9大类64个品种被列入第一批实施医疗器械唯一标识的产品目录。